广州医科大学附属妇女儿童医疗中心是华南地区规模最大的一所集预防、医疗、保健、科研、教学为一体的公立三级甲等妇女儿童专科医院;是国家儿童区域医疗中心(中南区域);国家建立健全现代医院管理制度试点医院及广东省高水平医院第二批重点建设医院。中心通过了国家电子病历评级七级评审、国家医疗健康信息互联互通标准化成熟度测评五级乙等评审。 2019年4月,中心互联网医院作为全省首批互联网医院之一,正式上线运营,实现儿童健康全方位管理等新型医疗服务模式,引领医疗服务创新。
一、机构简介
中心药物临床试验机构成立于2010年4月,设置有独立的办公室、专用档案室、药物临床试验中心药房。制订了79项药物临床试验相关的管理制度和SOP文件,基本涵盖了试验和GCP管理的各个环节,具备可操作性。根据新版GCP,完成了相应制度与SOP的修订。机构每年组织多种形式的GCP培训和学习,包括筹备大型的培训班、邀请专家现场指导、机构办公室内部培训等等,形式多样,内容丰富。
机构对临床试验项目实行全过程质控。质控分为二级,以保证临床试验数据的真实、准确、可靠。一级质控为专业组质控,专业负责人指定专人负责临床试验项目的质量控制,并向机构质控组长负责,随时对试验各环节进行监督、检查。二级质控为机构质控,机构质控员在试验前、中、后进行3次质控检查。
二、药物临床试验伦理委员会简介
中心药物临床试验伦理委员会成立于2010年7月,设置有独立的办公室、资料档案室以及相应的办公设备设施。已制定6项制度和26项标准操作规程。根据新版GCP,完成了相应制度和SOP的修订。现有主任委员1名,副主任委员1名,委员15名,秘书1名;委员中,医药相关专业11人,非医药专业6人,法律专家1人,院外社会人士2人,男女比例为10:7,均符合伦理委员会的组建要求,并在医学研究登记备案信息系统备案。伦理委员会每两个月召开一次审查例会,根据项目情况可增加会议频次;紧急会议随时召开。
三、药物临床试验已备案专业组简介
中心药物临床试验机构已备案17个药物临床试验专业组:妇科、小儿呼吸、小儿消化、小儿普通外科、小儿胸心外科、小儿血液科、小儿神经病学、产科、小儿内分泌、麻醉科、小儿传染病、小儿遗传病、新生儿、小儿免疫、小儿重症医学科、小儿肾病、儿童康复。各专业组人员均经过各级GCP培训并获得证书。各专业组配备了带锁专用药柜、冰箱;制定了符合本专业的制度、SOP,急救预案体系、质量管理体系、资料管理体系、药物管理体系。严格按照GCP相关法律法规开展临床试验。
四、医技辅助科室简介
中心医技辅助科室具备开展药物临床试验相关的检测、检验和诊断等相适应的仪器设备。检验科每年均参与卫生行政部门临床检验室室间质评,获得质评证书,并符合ISO 15189:2012《天博体育》(CNAS-CL02《天博体育》)的要求,获得中国合格评定国家认可委员会实验室认可证书。
附件:
1.地址及联系方式:
机构办公室:广州市华强路9号保利克洛维中盈大厦506室。
郑老师、祁老师,020-85596673,fezxgcp@gwcmc.org。
伦理委员会:广州市金穗路9号珠江新城院区住院部二楼。
周老师,020-38076262,gcplunli@gwcmc.org。
2.现场接待日:
机构办公室:除节假日外,周三、周四,上午8:00-12:00。
伦理委员会:除节假日外,周一至周五,上午8:00-12:00;下午2:00-5:00。
先电话预约,再现场递交伦理审查资料。
3.药物临床试验专业组已备案研究者查询:
网站:药物和医疗器械临床试验机构备案系统
药物备案查询网址:http://beian.cfdi.org.cn/CTMDS/apps/pub/drugPublic.jsp
医疗器械备案查询网址:http://beian.cfdi.org.cn/CTMDS/apps/pub/ylqxPublic.jsp
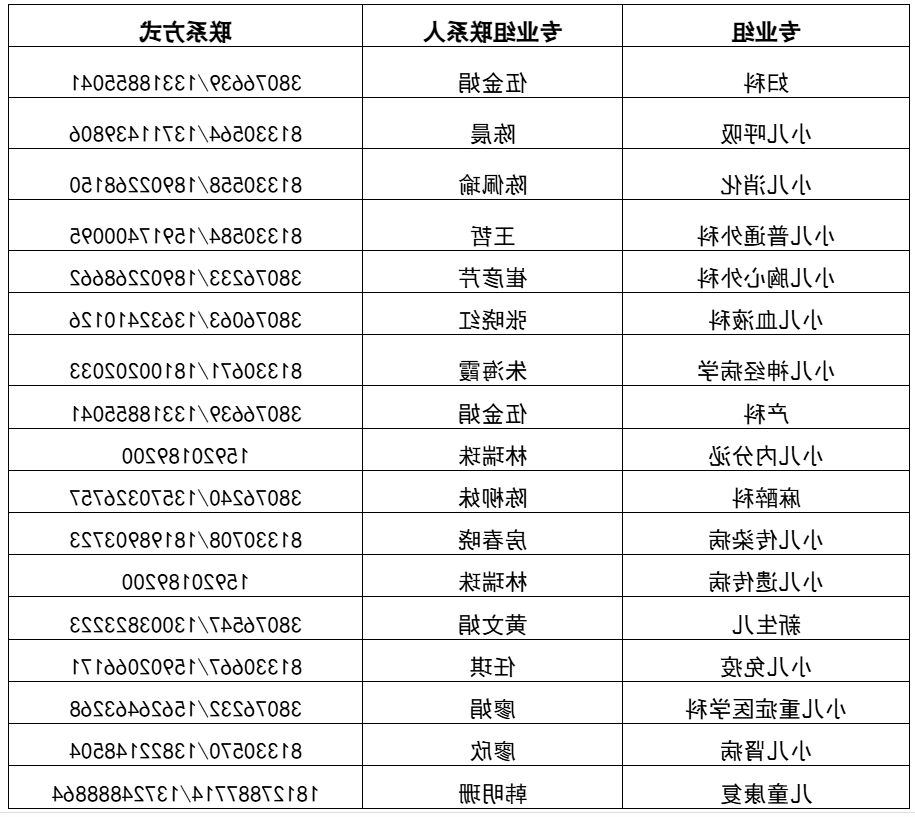
4.药物临床试验备案专业组联系人及方式:
附件:

 官方微博
官方微博